細胞膜に結合するペプチドによって人工細胞の変形を誘起することに成功!
細胞膜に結合するペプチドによって人工細胞の変形を誘起することに成功!
国立大学法人東京農工大学大学院工学研究院生命機能科学部門の川野竜司教授と同大学卓越大学院生 和泉佳弥乃、齋藤千尋は、人工細胞(リポソーム、注1)の変形を膜に結合するペプチドの二次構造によって誘起し、人工細胞を形状制御できる可能性を示唆しました。本技術は、目的に合わせて異なる形状に変形するリポソーム型分子ロボット(注2)への応用が期待されます。
本研究成果はMultidisciplinary Digital Publishing Instituteが発行するMicromachinesに2月2日に掲載されました。
https://www.mdpi.com/2072-666X/14/2/373
論文名: Liposome Deformation Induced by Membrane-Binding Peptides
著 者: Kayano Izumi, Chihiro Saito, and Ryuji Kawano
現状
私たちが日常的に利用している機械ロボットは複数の部品を組み合わせることで精密に制御され、高度な機能を発揮できるようになりますが、その小型化に課題があります。これに対して分子ロボット(注2)は、ナノサイズの分子を組み合わせて超小型ボディの中で機能を発揮させるシステムであり、生体内や土壌などの微小・混在環境での活用が期待できます。脂質二分子膜小胞であるリポソーム(注1)はその生体親和性の高さから分子ロボットのボディとしての活用が注目されています。リポソームは通常球形をしていますが、生体内や土壌などの微小・混在環境での効率的な移動にはその環境に応じて変形させる必要があります。これまでに界面活性分子や細胞骨格を構成するタンパク質を用いたリポソームの変形が報告されてきましたが、例えば任意の形状への変形などリポソームの精密な形状制御は難しく、分子ロボティクスにおける研究課題となっていました。
研究体制
本研究は、本学大学院工学府大学院生の和泉佳弥乃(FLOuRISH次世代研究者挑戦的研究プログラム生および卓越大学院生)、大学院生(当時)の齋藤千尋、工学研究院生命機能科学部門の川野竜司教授らによって実施されました。本研究はJSPS科研費挑戦的研究(萌芽)21K19786、学術変革領域研究(A)21H05229の助成を受けたものです。
研究成果
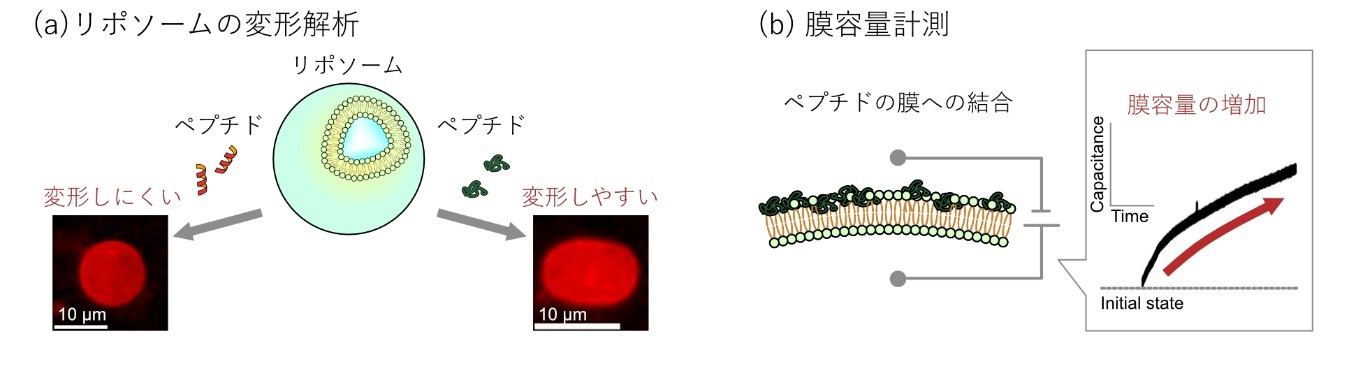
本研究では、近年設計や合成の方法論の進歩が著しいペプチドを変形材料として用い、ペプチドによるリポソーム変形の誘導と、その原理の解明を試みました。自発的に脂質二分子膜へ結合しうる膜結合性ペプチド4種類を添加したときのリポソーム形状変化を顕微鏡観察しました(図1a)。実験の結果、リポソームを変形させる能力が膜透過性ペプチド(CPPs)というペプチドを用いたときに高くなることが判明しました。また変形原理を解明するために、膜容量(注3)を計測し脂質二分子膜へのペプチドの結合評価を試みました(図1b)。計測の際に観察される膜容量変化はペプチドの膜への結合を反映しています。この変化を解析し、顕微鏡観察結果と相関づけることにより、リポソームの変形が膜へ結合するペプチドの量ではなく、脂質膜におけるペプチドの二次構造に依存することを示唆しました。
今後の展開
本研究によって、リポソームの膜変形を膜に結合するペプチドの二次構造によって制御できる可能性が示唆されました。最近では、人工的なペプチドの設計や合成研究が益々進展しており、精密な形状制御を起こす材料としての応用が期待できます。今後、目的に合わせて異なる形状に変形する分子ロボットへの展開を目指しています。
注1)リポソーム
ナノ~マイクロサイズの脂質二分子膜小胞。細胞膜モデルや薬物伝達システムの輸送体として利用されている。
注2)分子ロボット
ロボット工学の方法論を導入して分子を組織化し、高度な「感覚」・「知能」・「運動」を有するプログラム可能な人工分子システム。
注3)膜容量
脂質二分子膜の静電容量。測定により、膜の面積・厚さ・誘電率の変化を推定できる。

◆研究に関する問い合わせ◆
東京農工大学大学院工学研究院
生命機能科学部門 教授
川野 竜司(かわの りゅうじ)
TEL/FAX:042-388-7187
E-mail:rjkawano(ここに@を入れてください)cc.tuat.ac.jp
