従来制御が困難であったジエンへの位置選択的な水素ーケイ素結合の付加に成功
従来制御が困難であったジエンへの位置選択的な水素ーケイ素結合の付加に成功
国立大学法人東京農工大学大学院工学研究院 小峰伸之助教、三井達夫氏、菊池 秀氏、平野雅文教授らは、従来制御が困難であったジエンへの水素―ケイ素結合の付加の位置選択性を錯体触媒上のリン配位子をかえるだけで、自在にコントロールすることに成功しました。この手法を応用することにより、様々な有機ケイ素化合物の選択的合成を達成できるものと期待されます。
本研究成果は、アメリカ化学会Organometallics誌(12月14日付電子版)に掲載されました。
論文名: Ligand–Controlled Regiodivergent Hydrosilylation of Conjugated Dienes Catalyzed by Mono(phosphine)palladium(0) Complexes
URL:https://pubs.acs.org/doi/10.1021/acs.organomet.0c00597
現状
有機ケイ素化合物は無機と有機の性能を併せ持つ特徴的な物性を示すため、幅広い製品で使用され、 将来用途も期待されています。現在の世界の有機ケイ素化合物の市場規模は1兆5000億円程度であり、今後も増加が見込まれています。また、有機ケイ素化合物は、アルコールの合成や炭素―炭素結合の構築など有機合成試薬としても広く利用されています。炭素-炭素不飽和結合のヒドロシリル化反応(ここでは二重結合にケイ素と水素を付加する反応)は有機ケイ素化合物を与える反応であり、炭素-炭素二重結合を複数有する共役ジエンのヒドロシリル化反応では、炭素-炭素二重結合を有する有機ケイ素化合物が得られます。この反応ではケイ素の結合部位が異なる複数種の化合物(位置異性体)が生成する可能性がありますが、単一な位置異性体を選択的に作り分けることが望まれています。共役ジエンのヒドロシリル化反応により、単一な位置異性体を合成するために様々な金属種や複雑な構造を有する配位子が用いられてきましたが、これまで位置選択性を制御することは困難でした。
研究体制
本研究は、国立大学法人東京農工大学大学院工学研究院応用化学部門 小峰伸之助教、北里大学理学部 三井達夫氏 (外研生・卒業生)、同大学院生物システム応用科学府 菊池 秀氏(生物機能システム科学専攻博士後期課程修了生)、同大学院工学研究院応用化学部門 平野雅文教授らにより行われました。また、本研究は、JSPS科学研究費補助金 基盤研究(C) 20K05489の助成により行われました。
研究成果
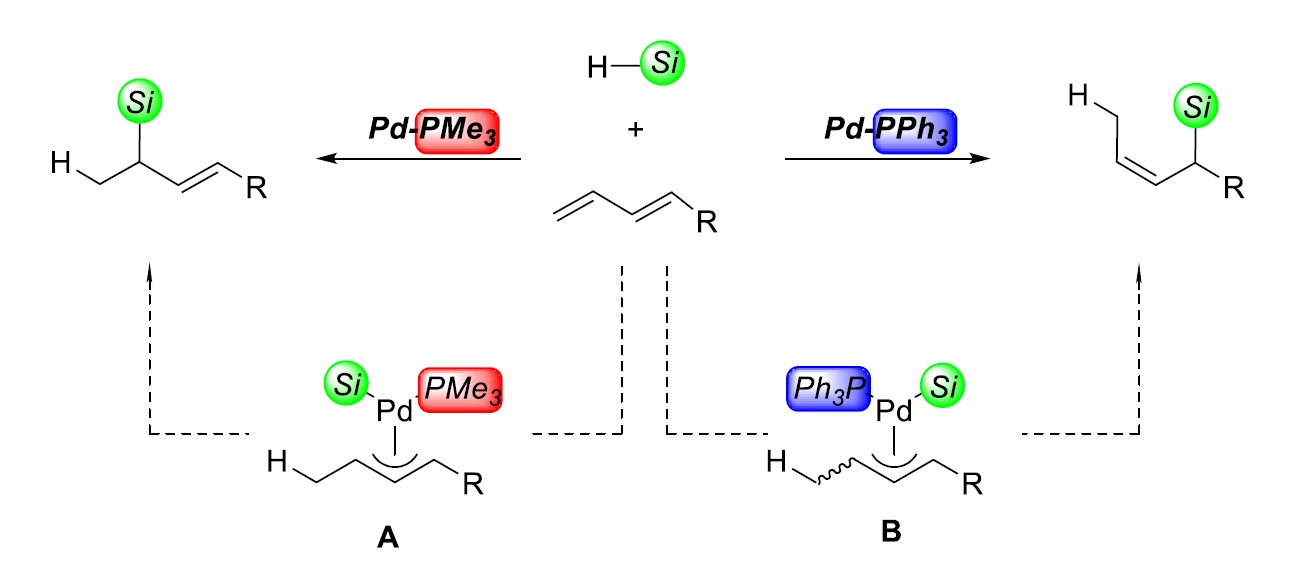
従来、不飽和化合物に水素―ケイ素結合を付加させるヒドロシリル化反応では、主に白金(プラチナ)触媒が用いられてきました。これまでに白金以外の錯体触媒を用いる研究も行われており、パラジウム錯体を触媒とする反応も知られていましたが、本研究では一分子のリン配位子を有するパラジウム錯体が、特異的にヒドロシリル化に高い活性を示すことを見出し、各種共役ジエンを用いたヒドロシリル化反応を行いました。この反応では一分子のリン配位子を有するパラジウム錯体を用いることで生成物が高収率で得られるだけでなく、赤色で示したトリメチルホスフィンも有するパラジウム錯体と青色で示したトリフェニルホスフィンも有するパラジウム錯体をそれぞれ使い分けることで、それぞれ別の構造を持った分子として選択的に作りわけることに成功しました(図1)。このことはリン配位子を使い分けることで反応中間体Aと反応中間体Bがそれぞれを選択的に生成させることにより達成できたものと考えられます。また、触媒はこれまで先行例の少ないエステル置換基を有するジエン類のヒドロシリル化反応も可能になりました。
今後の展開
これまで反応に用いられてきたジエンの置換基は主にアルキル基やアリール基であったのに対して、エステル基などの様々な置換基を有するジエンのヒドロシリル化反応に展開が期待されます。また、得られた生成物は、シリル置換基を利用したカップリング試薬やアリル化剤としての生理活性物質合成への応用やケイ素を含むポリマー原料としての利用が期待されます。
◆研究に関する問い合わせ◆
東京農工大学大学院工学研究院
応用化学部門 助教
小峰 伸之(こみね のぶゆき)
TEL:042-388-7541 FAX:042-388-7044
E-mail:komine(ここに@を入れてください)cc.tuat.ac.jp
関連リンク(別ウィンドウで開きます)
