ペプチドナノファイバーの集合構造と熱応答性の制御に成功―細胞接着性ヒドロゲルの新たな力学特性・温度応答性制御法の構築
ペプチドナノファイバーの集合構造と熱応答性の制御に成功
細胞接着性ヒドロゲルの新たな力学特性・温度応答性制御法の構築
東京農工大学大学院工学府応用化学専攻の石田敦也大学院生(修士2年)、東京農工大学大学院グローバルイノベーション研究院(工学部応用化学科 兼務)の村岡貴博准教授、東京医科歯科大学統合研究機構先端医歯工学創成研究部門脳統合機能研究センターの味岡逸樹准教授、北里大学理学部の渡辺豪助教、神奈川県立産業技術総合研究所の押川未央研究員、は、自己集合性ペプチドが形成するナノファイバーの集合構造と温度応答性を制御する新たな分子設計手法を開発しました。従来、集合構造を不安定化(ゲルの強度を低下)させると考えられていたアミノ酸の置換を特定の部位に行うことで、逆に集合構造を安定化(ゲルの強度を向上)させることができたのです。さらに温度によって液体(ゾル)と固体(ゲル)の状態を制御できました。ペプチドナノファイバーは細胞接着性を有し、生体の組織回復を促進するバイオ材料などとしての応用が期待されています。本研究で開発した手法は、ペプチド材料の重要な特性である力学特性や温度応答性などを精密に制御する上で役立つと期待されます。
本研究成果は、ドイツWiley-VCH社のChemistry–A European Journal誌電子版(7月8日付, doi: 10.1002/chem.201902083)に掲載されました。
URL: https://onlinelibrary.wiley.com/doi/10.1002/chem.201902083
現状
ペプチド(アミノ酸がつながった構造)でできたペプチドナノファイバー(注1)は、細胞培養材料や組織回復を促進する再生医療材料として利用されるヒドロゲル(注2)を構築します。このペプチドヒドロゲルを応用利用する際、目的に応じてその力学強度や温度応答性を制御することが求められるため、それらの特性を制御する技術は重要です。通常、力学強度の高いヒドロゲルを作成する場合、ゲルを構成するペプチドの疎水性を高め、ペプチド分子間の疎水性相互作用(注3)を強くする分子設計が行われます。例えば、アラニンをフェニルアラニンに置換する方法が知られています。しかしこの方法では、温度応答性が失われる場合が多く、力学強度の向上と温度応答性の保持を両立する一般的な分子設計手法は十分に確立されていないのが現状です。
研究体制
東京農工大学大学院工学府応用化学専攻の石田敦也大学院生(修士2年)、東京農工大学大学院グローバルイノベーション研究院の村岡貴博准教授、東京医科歯科大学脳統合機能研究センターの味岡逸樹准教授、北里大学理学部の渡辺豪助教、神奈川県立産業技術総合研究所の押川未央研究員が共同で実施しました。本研究は、科学研究費助成事業若手研究(A) (17H04885)、科学技術振興機構さきがけ「分子技術と新機能創出」、公益財団法人東電記念財団などの研究支援によって実施されました。
研究成果
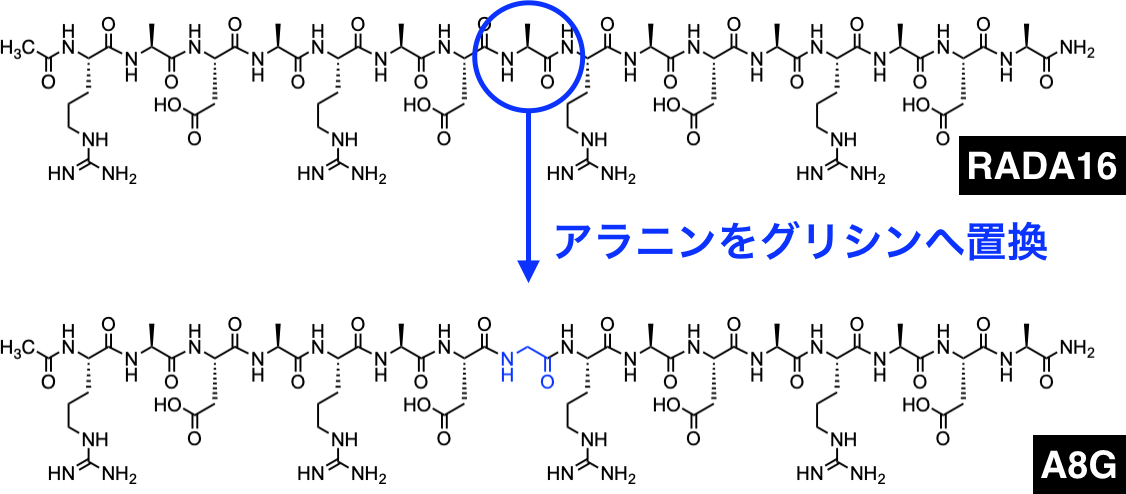
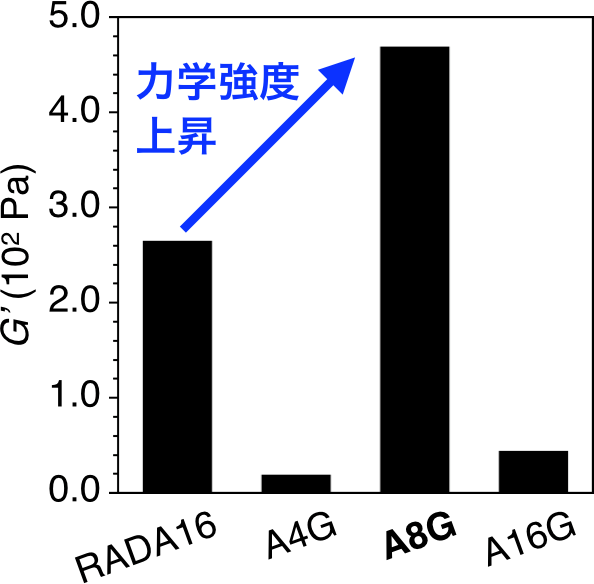
ナノファイバーを形成する両親媒性ペプチド(注4)の中に含まれるアラニンをグリシンに置換することによって、ヒドロゲルに温度応答性を付与し、ヒドロゲルの力学強度を上昇させることが可能であることを実証しました。グリシンへの置換はペプチド分子の柔軟性を高めるため、ナノファイバーなどのペプチド集合体構造を不安定化し、ヒドロゲルの力学強度を低下させると考えられています。しかし今回、両親媒性ペプチドの分子中央に位置するアラニンをグリシンに置換する手法は、例外的にヒドロゲルの強度を上昇させることを発見しました(図1,図2)。この力学強度の向上は、ナノファイバーのバンドル構造(束状構造)の形成に由来することも突き止め、加熱によりゲルからゾル(溶液)へ転移する温度応答性も見られたことから、ヒドロゲルの力学強度の向上と温度応答性の保持を両立する新手法として有効であることを実証しました(図3)。さらに今回、グリシンへの置換によるナノファイバーのバンドル化は、分子動力学シミュレーションによっても再現されました。このことから、他の両親媒性ペプチドに対してもグリシンへの置換による効果を計算によって予測することが可能であると考えられ、目的とする性質を持つペプチドヒドロゲルを計算科学によって設計する効率的なバイオ材料の開発につながると期待されます。
今後の展開
ペプチドヒドロゲルは、組織回復を促進する再生医療材料などとして注目されています。ペプチドヒドロゲルを応用利用する際には、目的に応じて力学強度を調節する必要があります。また温度変化によりゲルからゾルへ転移する温度応答特性は、注射による局所部位への投与を可能にします。両者の両立を可能にする今回開発した手法が、ペプチドヒドロゲルのバイオ材料としての利用の幅を広げ、高機能化、実用化に貢献すると期待されます。
注1)ナノファイバー
直径がナノメートルサイズの繊維状構造。今回の研究では、直径が3から5ナノメートル程度のペプチドナノファイバーの形成が確認された。
注2)ヒドロゲル
水を分散媒として含むゲル。ペプチドナノファイバーのような繊維状構造が水の中で絡まり合うことで作られる。
注3)疎水性相互作用
分子中の疎水性部分同士が、水中で水からはじかれる形で集合化する性質。
注4)両親媒性ペプチド
親水性アミノ酸と疎水性アミノ酸を両方含むペプチド。両親媒性ペプチドの多くは、水の中で集合し、ナノファイバーなどの分子集合体を形成する。

参考情報
・論文名:Glycine Substitution Effects on the Supramolecular Morphology and Rigidity of Cell‐Adhesive Amphiphilic Peptides
・掲載誌:Chemistry–A European Journal(ドイツWiley-VCH社)
・電子版掲載年月日:2019年7月8日
・著者名:A. Ishida, G. Watanabe, M. Oshikawa, I. Ajioka, T. Muraoka
・doi:10.1002/chem.201902083
◆研究に関する問い合わせ◆
国立大学法人東京農工大学
グローバルイノベーション研究院(工学部応用化学科 兼務)准教授
村岡 貴博(むらおか たかひろ)
TEL:042-388-7052
E-mail:muraoka(ここに@を入れてください)go.tuat.ac.jp
村岡研究室のホームページ:https://www.muraoka-lab.com
国立大学法人東京医科歯科大学
統合研究機構
先端医歯工学創成研究部門
脳統合機能研究センター 准教授
味岡 逸樹 (あじおか いつき)
TEL: 03-5803-4972
E-mail:iajioka.cbir(ここに@を入れてください)tmd.ac.jp
北里大学
理学部物理学科 助教
渡辺 豪(わたなべ ごう)
TEL:042-778-9540
E-mail:go0325(ここに@を入れてください)kitasato-u.ac.jp
地方独立行政法人神奈川県立産業技術総合研究所
研究開発部 常勤研究員(東京医科歯科大学脳統合機能研究センター常駐)
押川 未央 (おしかわ みお)
TEL:03-5803-4972
E-mail:oshikawa-mio.cbir(ここに@を入れてください)tmd.ac.jp
◆報道に関する問い合わせ◆
国立大学法人東京農工大学企画課広報係
TEL:042-367-5930
E-mail:koho2(ここに@を入れてください)cc.tuat.ac.jp
国立大学法人東京医科歯科大学総務部総務秘書課広報係
TEL:03-5803-5833
E-mail:kouhou.adm(ここに@を入れてください)tmd.ac.jp
学校法人北里研究所総務部広報課
TEL:03-5791-6422
E-mail:kohoh(ここに@を入れてください)kitasato-u.ac.jp
地方独立行政法人神奈川県立産業技術総合研究所
研究開発部研究支援課研究支援グループ
TEL:044-819-2034
E-mail:aoki(ここに@を入れてください)newkast.or.jp
