光パルスの整形技術で非染色分子イメージングの検出濃度限界を打破~生体中に埋もれた低濃度の薬剤が検出可能に~
光パルスの整形技術で非染色分子イメージングの検出濃度限界を打破
~生体中に埋もれた低濃度の薬剤が検出可能に~
【ポイント】
• 分子の濃度分布をそのままの状態で高速に画像化(イメージング)するコヒーレントラマン顕微鏡の検出限界濃度を従来の1/50に下げる新技術を開発しました。
• 生体分子に比べて薬剤分子の振動持続時間が長いことに着目し、レーザーパルスを薬剤分子の検出に最適な光波形に整形したことで、生体自身による背景光を抑えながら、薬剤分子を高いコントラストで撮像することに成功しました。
• 開発した光波形整形技術を応用した顕微鏡装置は、生命科学などの学術研究分野だけでなく、医薬品や化粧品などの産業分野への応用が期待できます。
東京農工大学大学院工学府の伊藤輝将特任助教、同大学院工学研究院の三沢和彦教授らの研究グループは、分子の濃度分布を標識や染色をせずにそのままの状態で高感度に撮影する「コヒーレントラマン顕微鏡」に独自の光波形整形技術を導入することにより、検出限界濃度を従来の1/50に下げる新技術を開発しました。生体中で低濃度の薬剤検出を可能にするこの技術は、非染色分子イメージングの適用範囲を拡大し、生命科学分野などの学術研究分野や医薬品や化粧品開発などの産業分野に大きく貢献することが期待されます。
本研究成果は米国物理学協会の国際学術誌APL Photonicsに2018年7月27日付で招待論文として掲載されました。招待論文とは、学術誌の編集委員会から執筆の依頼を受けて公表する論文のことで、専門分野におけるこれまでの貢献が認められて推薦されるものです。
Terumasa Ito, Yuki Obara, and Kazuhiko Misawa, "Spectral Focusing with Asymmetric Pulses for High-Contrast Pump–Probe Stimulated Raman Scattering Microscopy,"(高コントラストのポンププローブ誘導ラマン散乱顕微鏡を実現する非対称パルススペクトル集光)APL Photonics, Vol. 3, no. 9 (2018). Invited Article
https://aip.scitation.org/doi/10.1063/1.5030053(別ウィンドウで開きます)
研究の背景と経緯
小さな分子からなる化学物質(低分子化合物)は、生体機能を調節、維持する上で重要な働きを担っています。一般的に使われる医薬品も、そのほとんどは低分子化合物を有効成分とするものです。生体中の小さな分子の機能を理解するには、その濃度分布を細胞や組織の中でリアルタイムに追跡できるイメージング技術が重要になります。ところが、小分子の濃度分布は簡単には見えません。特定の分子を観察する手段としては、目的の分子に蛍光分子を結合させる「蛍光標識」が一般的によく使われています。しかし、蛍光分子自体が大きな分子量を持つために、低分子化合物本来のふるまいを変えてしまう、といった問題があります。
近年、標識を使わずにレーザーの照射だけで分子の濃度分布を高速撮影できる「コヒーレントラマン顕微鏡」と呼ばれる非染色イメージング技術が注目されています。これは、光が分子を通過するとき、分子が振動している影響を受けて色の変化した光がわずかに出てくる現象(ラマン散乱)を利用するものです。コヒーレントラマン顕微鏡では、瞬間的に発光するパルスレーザーを照射して、分子を強制振動させることで強いラマン散乱光を発生させます。このとき、どの程度色がずれた光が出てくるかは分子構造で決まるため、色ごとの散乱光の強さを見れば、どの化学物質がどれだけの濃度で含まれているかがわかります。この原理を利用すれば、レーザービームを測定試料の中で走査するだけで薬剤の濃度分布を撮影できる顕微鏡が実現できます。研究グループでは、このコヒーレントラマン顕微鏡の実用化に向けて技術開発を進めてきました。
〔2017年4月25日 本学プレスリリース〕
しかし、コヒーレントラマン顕微鏡に限らず、ラマン散乱を検出する従来の顕微鏡では、非染色であるがゆえに、生体組織に多く含まれる脂質や水などの分子の振動によるラマン散乱光も一緒に背景光として検出されてしまうという根本的な問題がありました。このため、生体の中で低い濃度の薬剤を撮影する際には画像のコントラストを上げることができず、検出可能な分子の濃度は制限されていました。
研究成果の概要
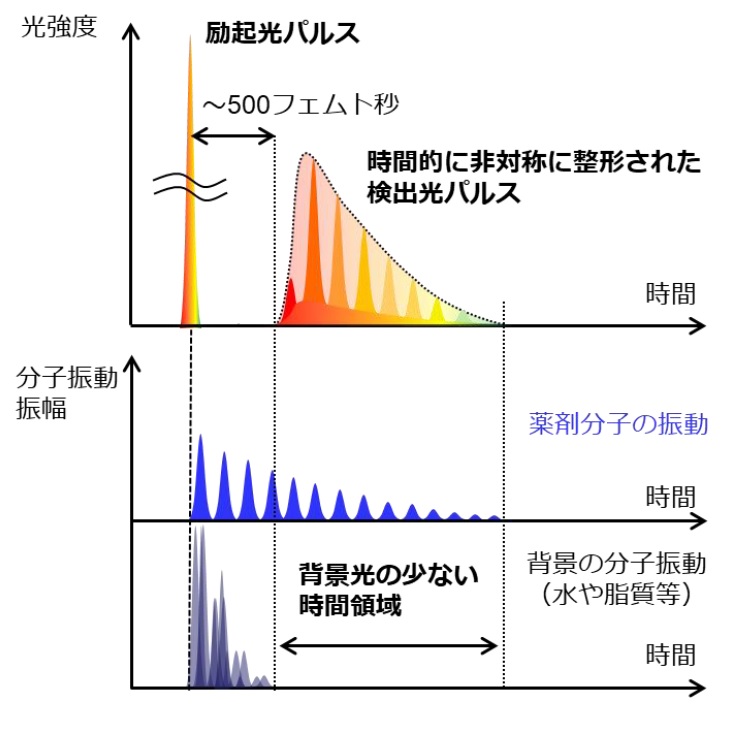
研究グループは、小分子薬剤と、生体組織に多く含まれる水や脂肪等の成分との間で分子振動の持続時間に違いがあることに注目しました(図1)。コヒーレントラマン顕微鏡では、超短パルス光を分子に照射して振動を開始させてから、続けて検出のためのパルス光を照射することで分子振動によるラマン散乱信号を取得します。ここで、振動を開始した直後に検出パルス光を当てると、組織自体に多く含まれる水分子や脂肪分子が強く振動するため、その背景光によって薬剤の信号が埋もれてしまいます。一方、わずかな時間だけ後の500フェムト秒以降(1フェムト秒=1000兆分の1秒)の領域では、組織自体の分子振動が減衰して背景光は小さくなるのに対し、薬剤分子の振動の中には比較的長く続くものも有ります。この性質を利用すると、薬剤分子の振動が消える前に、急峻に光強度が立ち上がる検出パルスを当てることで背景光だけを除去することが可能になります。ただし、単に検出パルスの時間幅を短くしてしまうと、近い周期で振動する分子同士を識別する性能(分解能)が低下するという別の問題が出てきます。
そこで研究グループは、光強度が急峻に立ち上がり、その後緩やかに減少する「非対称な時間波形」に整形された検出光パルスを使うことで、振動開始直後の背景光を回避しながら薬剤の信号を高コントラストかつ高い分解能で取得する独自技術を開発しました。この光波形整形は、検出パルスが光学フィルタ素子を通過するときに起こる非対称な時間広がりの効果を応用することで実現されました。
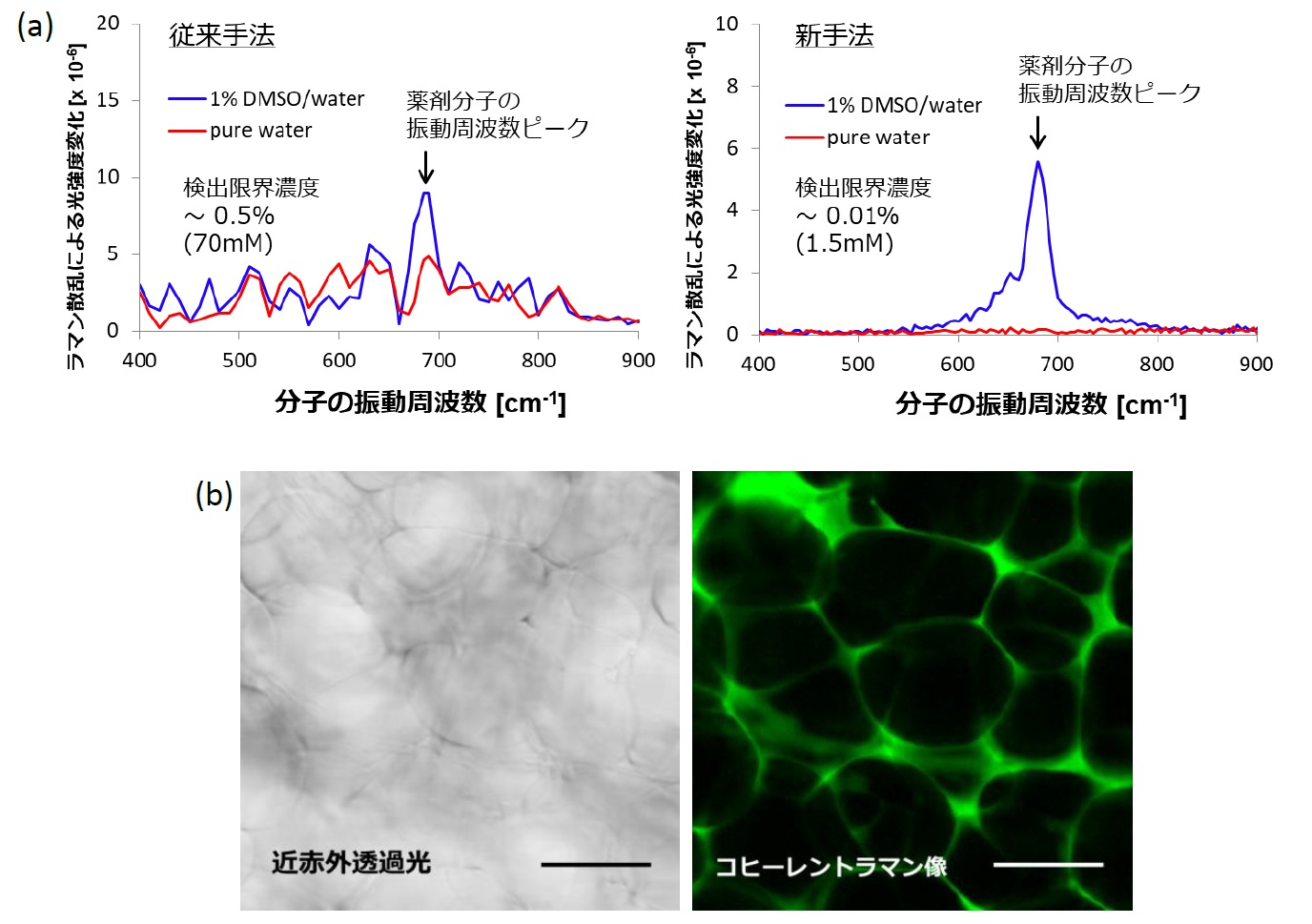
新手法を適用することで、コヒーレントラマン顕微鏡における検出可能な分子の濃度を従来の1/50に下げることに成功しました(図2(a))。また、脂肪組織に小分子薬剤を塗布して撮影したイメージング実証実験では、組織自体に由来する背景光が抑制され、細胞の周囲に浸透した薬剤分布を高いコントラストで撮影できることが確認されました(図2(b))。
今後の展開
これまでの非染色の分子イメージング技術は、生体自体に由来する背景光のため、原理的に検出限界濃度を下げることが難しく、応用範囲が限定されていました。今回開発した光波形整形技術によって検出限界が打破されたことで、細胞や組織中に低い濃度で存在する小分子薬剤であっても、空間分布やその時間変化を捉えることが可能になります。このイメージング技術は、生命科学分野をはじめとする学術研究分野、医薬品や化粧品の開発等の産業分野に広く貢献することが期待されます。
〔2017年4月25日リリース〕
染色不要で小さな分子の濃度分布を撮影できる顕微鏡を開発
~レーザ1台で動作するコヒーレントラマン顕微鏡の撮影速度を200 倍以上高速化~
https://www.tuat.ac.jp/outline/disclosure/pressrelease/2017/20170425_01.html
◆研究に関する問い合わせ◆
東京農工大学大学院
工学研究院 先端物理工学部門
教授 三沢 和彦(みさわ かずひこ)
E-mail:kmisawa(ここに@を入れてください)cc.tuat.ac.jp
