血管にかかる力を再現する三次元培養血管モデルを開発 – ステント留置を可能にし、次世代ステント設計に貢献 –
血管にかかる力を再現する三次元培養血管モデルを開発
– ステント留置を可能にし、次世代ステント設計に貢献 –
国立大学法人東京農工大学大学院工学府生体医用システム工学専攻博士前期課程の奥野拓 氏(研究当時)、同大学院グローバルイノベーション研究院の吉野大輔 教授、同大学院工学研究院先端物理工学部門の伊藤一陽 助教は、国立大学法人東北大学流体科学研究所の船本健一 教授との共同研究により、ステントを実際に留置できる三次元培養血管モデルを開発し、生理的な血流環境下でステント留置後の内皮化過程を定量的に評価することに成功しました。本研究では、血管モデルの設計・作製から細胞培養、血流負荷、ステント留置、評価手法までを一連の実験系として体系的に構築し、その詳細なプロトコルを論文中に明示しています。これにより、ステントが血管壁に与える力学的作用と、それに応答する血管内皮細胞の動態を同一条件下で統合的に解析することが可能となりました。
本成果は、再狭窄や血栓症の発生機序の理解を深めるとともに、次世代ステント設計の最適化に資することが期待されます。
本研究成果は、BMC Methods(5月12日付)に掲載されました。
論文名:Cell-cultured PDMS vascular model to allow placement of implant devices
URL:https://doi.org/10.1186/s44330-026-00072-9
本論文に関連するプレプリント
プレプリントURL: https://doi.org/10.1101/2025.01.20.634010
背景
動脈硬化などによる血管狭窄に対して、ステント留置は広く行われている治療法です。しかし、ステントと血管壁の硬さの違いにより血管壁へ過度な機械的刺激が加わると、炎症や血栓形成、再狭窄(注1)を引き起こす可能性があります。ステント治療の長期的な成功には、留置後に血管内皮細胞(注2)がステント表面を速やかに被覆する「内皮化(注3)」の進行が重要です。このようなステントと血管の相互作用を理解するためには、血流環境下でステント留置後の血管応答を再現・評価できる実験系が必要です。しかしこれまで、
- 実際にステントを留置できる血管モデルが限られていた
- 血流によって生じる力の作用を十分に再現できなかった
- 力学環境と細胞応答を統合的に定量評価する実験系が確立していなかった
といった課題がありました。
研究体制
本研究は、上原記念生命科学財団(2020年度研究奨励金)の支援の下、東京農工大学と東北大学で実施されました。
研究成果
本研究では、ポリジメチルシロキサン(PDMS)製の三次元血管モデルを開発し、その内腔にヒト頸動脈由来血管内皮細胞を播種することで、円筒状の内皮単層を形成しました。
灌流装置を接続して血流環境を再現した状態で培養した結果、内皮細胞は流れの方向に沿って伸長・配向し、生体内に近い応答を示しました(図1)。また、血流条件の違いにより細胞脱落率が変化することも明らかとなり、血管にかかる力の影響を定量的に評価できることが示されました。
さらに、ニッケルチタン合金製の自己拡張型ステントをモデル内へ留置し、血流環境下で培養を継続しました(図2)。その結果、留置24時間後に約20%、48時間後に約50%のステント側面が血管内皮細胞で覆われ、内皮化することを示しました(図3)。
本研究は、ステント留置後の内皮細胞の移動・接着・被覆の過程を三次元的かつ定量的に解析できる実験系を提示した点に特徴があります。また、装置構成や実験条件を具体的に示すことで、ステントと血管壁の力学的相互作用(注4)を評価するための実践的手法を提案しています。
今後の展開
今後は、血管平滑筋細胞を含む多層構造モデルへの発展や、より生体に近い弾性特性を有する材料の導入を進めることで、血管壁の力学環境をより精緻に再現していきます。また、ステントと血管壁との間に生じる応力分布の可視化技術と組み合わせることで、再狭窄の発生機序の解明およびステント設計の最適化に資する評価系へと発展させていく予定です。
用語解説
注1)再狭窄
治療によって拡張した血管が再び狭くなる現象。血管壁の過剰な細胞増殖や炎症が関与する。
注2)血管内皮細胞
血管の最も内側を覆う細胞層を構成する細胞。血流に直接さらされ、血管機能の維持に重要な役割を果たす。
注3)内皮化
ステント留置後に血管内皮細胞がステント表面を覆う現象。十分な内皮化は血栓形成や再狭窄の抑制につながる。
注4)力学的相互作用
ステントと血管壁との間に生じる機械的な作用と、それに対する血管側の応答の関係。
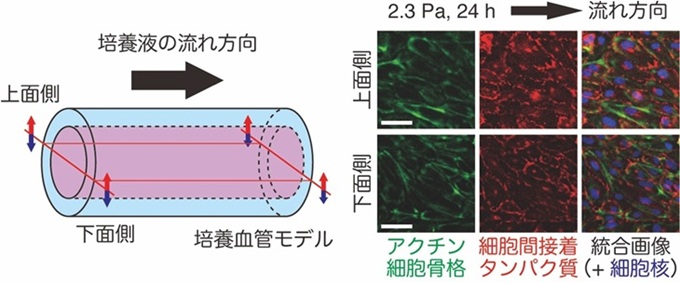
図1:培養血管モデル内部を単層で覆う血管内皮細胞の免疫蛍光染色画像。2.3 Paのせん断応力を24時間負荷した後、血管モデルを上下に切り分けて染色、観察したもの。血流を模擬した培養液の流れに応答し、血管内皮細胞が流れ方向に並び、伸びている様子が観察できる。スケールバーは50 µmを示す。図は(Okuno et al, 2026. BMC Methods, 3, 16)を改変して吉野らにより作成。
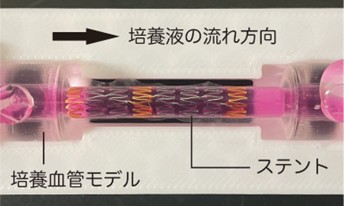
図2:開発した培養血管モデルにニッケルチタン合金製の自己拡張型ステントを留置した様子。図は(Okuno et al, 2026. BMC Methods, 3, 16)を改変して吉野らにより作成。
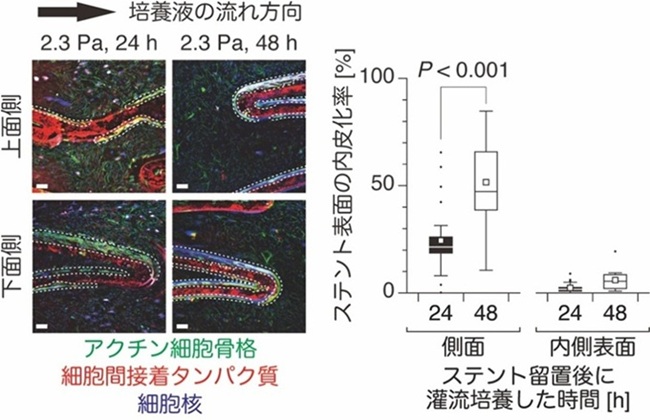
図3:ステントの内皮化。培養血管モデルの内側表面の血管内皮細胞が増殖しながらステントの側面を覆っていく様子が観察できる(白い波線で囲んだ部分が血管内皮細胞がステント表面を覆っている部分を示す)。スケールバーは100 µmを示す。図は(Okuno et al, 2026. BMC Methods, 3, 16)を改変して吉野らにより作成。
◆研究に関する問い合わせ◆
東京農工大学大学院グローバルイノベーション研究院
教授 吉野 大輔(よしの だいすけ)
TEL/FAX:042-388-7113
E-mail:dyoshino(ここに@を入れてください)go.tuat.ac.jp
◆報道に関する問い合わせ◆
東京農工大学 総務課広報室
E-mail:koho2(ここに@を入れてください)cc.tuat.ac.jp
東北大学流体科学研究所 国際研究戦略室(広報)
E-mail:ifs-koho(ここに@を入れてください)grp.tohoku.ac.jp
関連リンク(別ウィンドウで開きます)
- 東京農工大学 吉野大輔教授 研究者プロフィール
- 東京農工大学 伊藤一陽助教 研究者プロフィール
- 東京農工大学 吉野大輔教授、伊藤一陽助教 研究室WEBサイト
- 吉野大輔教授、伊藤一陽助教が所属する 東京農工大学工学部生体医用システム工学科
